경제
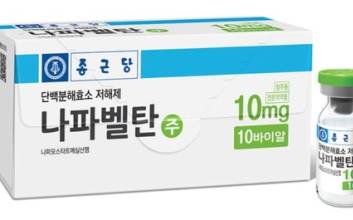
종근당 코로나 치료제 허가 불발, 멀고 먼 국산 2호 치료제 탄생
2호 국산 코로나19 치료제 탄생이 미뤄졌다. 종근당이 개발하고 있는 코로나19 치료제 '나파벨탄주'의 조건부 허가가 불발됐다. 식품의약품안전처는 18일 전날 첫 번째 전문가 자문회의인 검증 자문단 회의 결과, 조건부 허가가 적절하지 않다는 의견이 나왔다고 밝혔다. 식약처는 더는 자문 절차를 진행하지 않고 임상 3상 시험을 지원할 방침이다. 종근당의 나파벨탄주는 췌장염 치료제로 쓰던 전문의약품이다. 러시아에서 임상 2상 시험을 진행하고 이달 8일 식약처에 조건부 허가를 신청했다. 나파벨탄에 코로나19 치료 효능·효과를 추가하기 위한 변경 허가를 신청한 것이다. 검증 자문단은 환자 104명을 대조군 51명과 시험군 53명으로 나눠 수행한 임상 2상 시험 자료를 검토했다. 임상에서 나파벨탄주를 시험군에 10일간 투여한 결과 임상적 개선 시간이 시험군과 대조군 모두 11일로 차이가 나타나지 않아 유효성을 입증하지 못했다는 결론을 냈다. 바이러스 검사 결과가 양성에서 음성으로 전환되는 시간도 시험군과 대조군 모두 4일로 차이가 없었다. 일부 중증 고위험군에서는 시험군과 대조군 간에 통계적 유의성이 나타났다. 하지만 자문단은 이 임상시험이 해당 환자군을 대상으로 계획되지 않았다고 지적했다. 검증 자문단은 임상 2상 결과만으로는 이 약의 치료 효과를 인정하기 충분하지 않아 효과를 확증할 수 있는 추가 임상이 필요하다는 의견을 냈다. 이에 종근당은 3상 시험을 통해 효과를 입증하겠다고 밝혔다. 셀트리온이 개발한 항체치료제 렉키로나주가 국산 1호 코로나 치료제다. 2호 치료제로 종근당이 유력했지만 식약처의 1차 관문도 통과하지 못했다. GC녹십자와 대웅제약이 2호 치료제 후보로 꼽히고 있다. GC녹십자는 코로나 혈장치료제 허가 신청을 위해 임상 2상에 집중하고 있다. GC녹십자 관계자는 “1분기 안에 분석을 완료한 뒤 4월에는 식약처에 허가를 신청할 예정”이라고 밝혔다. GC녹십자는 지난해 12월 임상 2상 시험 대상자에 대한 투약을 마치고 데이터를 분석 정리하고 있다. 특히 혈장치료제는 실제 의료 현장에서 치료 목적으로 쓰이고 있다. 지난해 10월부터 총 41건의 치료목적 사용 승인을 받았다. 대웅제약은 경구형 치료제 호이스타정을 코로나19 치료제로 개발하기 위해 임상을 진행 중이다. 하지만 대웅제약 역시 종근당처럼 임상 2상에서 유의미한 결과를 내지 못했다는 평가를 받고 있다. 이외 부광약품, 신풍제약, 크리스탈지노믹스, 동화약품, 이뮨메드, 녹십자웰빙 등이 코로나 치료제 개발을 위한 임상 2상 시험을 하고 있다. 그렇지만 업계에서는 코로나 백신 접종이 활발하게 이뤄지고 있기 때문에 코로나 치료제 개발에 대한 동력이 무뎌졌다는 평가하고 있다. 업계 관계자는 “임상 3상은 많은 비용이 들어가고 성공 확률도 통상 10% 미만이라 조건부 허가를 받지 못한 제약사가 시도하기 쉽지 않다”고 말했다. 김두용 기자 kim.duyong@joongang.co.kr
2021.03.18 16:39








![공정위, 대기업 분석팀 신설 “일감몰아주기 의심되면 직권조사”[only 이데일리]](https://image.edaily.co.kr/images/Photo/files/NP/S/2026/01/PS26012000018T.jpg)




![[포토]최우식, 패션위크 위해 파리 출국](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000128.400x280.0.jpg)
![[포토]최우식, 몰아치는 강풍에 깜짝!](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000127.400x280.0.jpg)
![[포토]최우식, 춥다 추워!](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000126.400x280.0.jpg)
![[포토]최우식, 추워진 날씨에 잔뜩 웅크린 어깨](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000125.400x280.0.jpg)
![[포토]최우식, 남친룩의 좋은 예](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000124.400x280.0.jpg)
![[포토]최우식, 눈웃음에 무장 해제](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000123.400x280.0.jpg)
![[포토]최우식, 애교 장인의 하트](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000122.400x280.0.jpg)
![[포토]최우식, 파리 잘 다녀올게요](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000121.400x280.0.jpg)
![[포토]최우식, 장난꾸러기 미소](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000120.400x280.0.jpg)
![[포토]최우식, 하트에서 꿀이 뚝뚝](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000119.400x280.0.jpg)
![[포토]최우식, 애교장인](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000118.400x280.0.jpg)
![[포토]세븐틴 민규, 엔딩포즈같은 출국길 인사](https://image.isplus.com/data/isp/image/2026/01/19/isp20260119000113.400x280.0.jpg)
