산업
마스크 벗자 독감 환자 급증, 다시 불붙은 녹십자와 SK의 '독감 백신 시장'
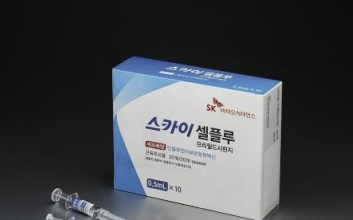
마스크 의무 해제와 맞물려 독감 환자가 증가하고 있다. SK바이오사이언스는 코로나19 백신 생산으로 멈췄던 독감 백신 생산을 재개했다. 이에 ‘독감 백신 시장’에 대한 관심이 다시 쏠리고 있다. 17일 질병관리청의 감염병 표본감시 주간소식지에 따르면 올해 14주차(4월2일~4월8일) 외래환자 1000명당 인플루엔자 의심 증상을 보이는 환자의 분율(인플루엔자 의사환자 분율)은 15.2명으로 전주(14.5명)보다 늘었다. 최근 8주차 11.6명까지 떨어졌던 환자의 분율은 6주 만에 3.6명까지 증가한 것이다. SK바이오사이언스는 최근 독감 백신 원액 생산에 돌입했다. 지난달 세계보건기구(WHO)가 올해와 내년에 유행할 것으로 예상되는 독감 바이러스 균주를 공개하면서 독감 백신 사업에 다시 시동을 건 것이다. SK바이오사이언스의 4가 독감백신 '스카이셀플루4가프리필드시린지'는 GC녹십자의 '지씨플루쿼드리밸런트프리필드시린지'와 함께 독감 백신 시장에서 양대 산맥을 이루고 있었다.스카이셀플루는 세포배양 방식의 4가 독감 백신이며 지씨플루는 유정란을 활용한 4가 백신이다. SK바이오사이언스는 2020년 독감 백신 생산 1위에 오른 바 있다. 그러다 2021년 SK바이오사이언스가 코로나19 백신에 집중하면서 GC녹십자에 1위 자리를 내준 바 있다.
GC녹십자는 SK바이오사이언스가 코로나 백신에 집중하는 사이 독감 백신 매출액이 40% 가량 성장했다. 이로 인해 1위 수성에 최선을 다한다는 계획이다. 다시 제 자리로 돌아온 SK바이오사이언스는 독감 백신 시장에 욕심을 낼 수밖에 없는 상황이다. 회사는 최근 칠레에서 스카이셀플루의 품목허가를 받으며 사업 영역 확장에 나섰다.안재용 SK바이오사이언스 사장은 "올해 생산이 재개되는 스카이셀플루는 이미 검증된 제품 경쟁력을 기반으로 국내를 넘어 글로벌로 영역을 확대해 나갈 예정"이라며 의지를 드러내기도 했다. 김두용 기자 k2young@edaily.co.kr
2023.04.17 10:29













![보험금 10배 올리고 사망한 '시한부 여동생'…마지막 선물의 진실[그해 오늘]](https://image.edaily.co.kr/images/Photo/files/NP/S/2026/03/PS26030200003T.jpg)
![영원한 강자 없다(?)...시험대 오른 비만약 제왕 노보노디스크 [클릭, 글로벌 제약·바이오]](https://image.edaily.co.kr/images/Photo/files/NP/S/2026/03/PS26030100377T.jpg)




![[포토] 인사말 하는 이승훈](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000133.400x280.0.jpg)
![[포토] 인사말 하는 빠니보틀](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000132.400x280.0.jpg)
![[포토] 인사말 하는 김무열](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000131.400x280.0.jpg)
![[포토] 인사말 하는 비](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000130.400x280.0.jpg)
![[포토] '크레이지 투어', 꼭 본방사수 부탁드려요~](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000129.400x280.0.jpg)
![[포토] '크레이지 투어', 화이팅](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000128.400x280.0.jpg)
![[포토] '크레이지 투어', 기대해도 좋아요](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000125.400x280.0.jpg)
![[포토] '크레이지 투어', 색다른 조합](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000126.400x280.0.jpg)
![[포토] '크레이지 투어', 네 남자의 케미 기대해 주세요](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000127.400x280.0.jpg)
![[포토] '크레이지 투어' 연출한 송가희 PD](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000123.400x280.0.jpg)
![[포토] '크레이지 투어' 연출한 오동인 PD](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000124.400x280.0.jpg)
![[포토] '깡' 포즈 취하는 이승훈, '지훈이 형 보고 있어요?'](https://image.isplus.com/data/isp/image/2026/02/27/isp20260227000118.400x280.0.jpg)
